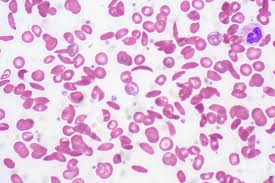
 疟疾,特别是恶性疟,给人类基因组施加了很大的选择压力。镰状血红蛋白突变使血红蛋白A中β珠蛋白链上的6位谷氨酸突变为缬氨酸,从而产生血红蛋白S。在一个确定的平衡多态体系中,那些纯合突变的人会因血红蛋白基因的突变而饱受镰形红细胞贫血的困扰,而杂合突变(拥有血红蛋白AS)的人就比较幸运了,杂合突变对他们的血红蛋白功能几无影响,并且他们在感染严重的恶性疟后症状轻微,且较正常人有更强的抵抗力。Ferreira团队的一项最新研究深入揭示了血红蛋白AS在抵抗疟疾方面的作用机制,因此也提供了一种防治疟疾的潜在手段。
疟疾,特别是恶性疟,给人类基因组施加了很大的选择压力。镰状血红蛋白突变使血红蛋白A中β珠蛋白链上的6位谷氨酸突变为缬氨酸,从而产生血红蛋白S。在一个确定的平衡多态体系中,那些纯合突变的人会因血红蛋白基因的突变而饱受镰形红细胞贫血的困扰,而杂合突变(拥有血红蛋白AS)的人就比较幸运了,杂合突变对他们的血红蛋白功能几无影响,并且他们在感染严重的恶性疟后症状轻微,且较正常人有更强的抵抗力。Ferreira团队的一项最新研究深入揭示了血红蛋白AS在抵抗疟疾方面的作用机制,因此也提供了一种防治疟疾的潜在手段。
恶性疟原虫感染的表现不尽相同,轻者可有无症状的寄生虫血症,重者则常常致死。反复的寄生虫感染使流行地区逐渐获得免疫力,但是抗疟免疫的机制尚知之甚少。另外,有些感染仅从无症状的寄生虫血症发展至简单的发热性疾病,而另一些感染则可导致严重的临床表现,个中原因尚未明了。
Ferreira团队使用了一个不错的镰形红细胞贫血的动物模型来研究血红蛋白AS的抗疟机制,在这个模型中,小鼠表达拥有镰形突变和两个附加突变的人β珠蛋白。研究者用啮齿类动物寄生虫——伯氏疟原虫感染小鼠,以引起类似人脑型疟疾(人恶性疟的一种严重表现)的严重感染。正如在预实验中所见,当小鼠感染伯氏疟原虫后,突变型小鼠脑型疟疾的发生率明显低于野生型小鼠。Ferreira团队认为镰形细胞突变抗疟作用的机制在于其耐受性提高而非抵抗力提高,因为突变型和野生型接受的寄生虫剂量是一致的,但突变型却能够避免脑型疟发病。这种保护作用基于一种能够降解游离亚铁血红素的酶——血红素氧化酶-1的诱导作用,游离亚铁血红素因此不能聚集,从而阻止了疟疾向着严重的方向发展。
然而此文作者评论说:Ferreira团队的这项研究在阐明血红蛋白AS抗疟的机制方面有其局限性。首先,转基因小鼠只提供了关于人类疾病的一个很粗糙的模型,特别是在血红蛋白AS抵抗严重疟疾的自然性方面更是如此。第二,小鼠感染的伯氏疟原虫和人感染的恶性疟原虫有所不同,能否由基于小鼠感染伯氏疟原虫的研究推广至人脑型疟尚存争议。第三,小鼠的镰形突变或许不能完全代表人类的血红蛋白AS;在小鼠中,对脑型疟的抵抗力并不伴随寄生虫载量的降低,但多数研究都发现,在人类中感染疟疾后,无症状的血红蛋白AS型患者的寄生虫载量较血红蛋白正常的人为低。
尽管存在局限性, Ferreira团队的研究仍然提供了防治疟疾的新思路。在严重疟疾的治疗方面,基于血红素氧化酶或一氧化碳的药物可能延缓快速进展的疾病进程,因此其具备了挽救生命的潜能。尽管如此,对疟疾患者的治疗仍将着重于对寄生虫的快速清除方面;就这一点而言,最近静脉内注射快速反应青蒿素这一标准治疗的建立是一项重大的进展。
在疟疾的预防方面,这项研究提示除了抗寄生虫药物之外,宿主因素在预防疾病的进展方面有着重要作用。人们已经设计出了一些通过防止蚊子叮咬从而预防疟疾的方法,比如使用用杀虫剂浸泡过的床帘或在市内喷洒杀虫剂,但是这样做也会降低对疟疾的获得性免疫力和寄生虫介导的耐受性,进而使人们患病时病情更为严重。其他预防手段,比如直接对抗孢子或肝脏期寄生虫的疫苗和间断预防性治疗或化学预防(能够杀死红细胞中的寄生虫而非肝脏期寄生虫)的药物允许寄生虫感染的存在,并因此获得耐受力和免疫力,以使疟原虫感染不致出现症状。重要的是,即便应用药物预防由于红细胞内寄生虫导致的疾病,宿主对肝脏期寄生虫的反应仍然能够提供足够的保护功效。这提示允许早期不出现症状感染存在的疫苗或药物,对预防潜在的致死性疟疾而言是一种很有希望的方式,并且这种方式并不会消除抗疟药的作用。
尽管距离消灭疟疾还有很长的路要走,但预防疟疾的手段正在全世界范围内推广。在上面的例子中,血红蛋白AS基因型的存在也是人类进化的一种方式,现在人们对这种方式有了更为深刻的理解。这种保护患者免受严重疟疾侵害的方式提供给我们一种新策略,它或许能治疗严重的疟疾并减少其发生率,但同时也并不增加感染者发展至严重疾患的几率。
本文编译自:《新英格兰医学杂志》2011-6-30 基础研究的临床意义
Philip J. Rosenthal, M.D. Lessons from Sickle Cell Disease in the Treatment and Control of Malaria. NEJM 364;26.
图片来源: euthman
