本文要点:乳腺癌,是女性最常见的恶性肿瘤,而三阴乳腺癌,又是其中预后较差的一种。本期《新英格兰医学杂志》,就刊登了这样一篇研究,一种新型的PARP抑制剂Iniparib与化疗联合应用,治疗三阴乳腺癌。本文从最基本的理论知识,到研究的设计与结果,最后又将本期的编辑述评加以总结,对这一问题进行了讨论。最终表明,Iniparib与化疗联合,可以明显的改善转移性三阴乳腺癌的预后。
 乳腺癌,是女性最常见的恶性肿瘤,现在已经得到了越来越多的重视。平日里,医生或者身边有着良好预防保健观念的人都会告诉女性们,要注重乳房的保健,定期的体检以及自我检查,对于早期发现乳腺癌、尽早治疗、改善预后有着非常重要的作用。(前些日子NEJM的一项研究报道称,在挪威,各项预防措施中,钼靶摄像筛查对乳腺癌死亡率的减低的作用仅占1/3。) 不过,这并不是今天文章的重点。上面的引子,只是想告诉大家,乳腺健康,对于每一位女性都是非常重要的。
乳腺癌,是女性最常见的恶性肿瘤,现在已经得到了越来越多的重视。平日里,医生或者身边有着良好预防保健观念的人都会告诉女性们,要注重乳房的保健,定期的体检以及自我检查,对于早期发现乳腺癌、尽早治疗、改善预后有着非常重要的作用。(前些日子NEJM的一项研究报道称,在挪威,各项预防措施中,钼靶摄像筛查对乳腺癌死亡率的减低的作用仅占1/3。) 不过,这并不是今天文章的重点。上面的引子,只是想告诉大家,乳腺健康,对于每一位女性都是非常重要的。
而就现在的医疗水平而言,在众多恶性肿瘤中,乳腺癌的预后可以说还是相当不错的,而且随着各项研究的不断进步,人类也正在朝着攻克乳腺癌的方向不懈努力。但就在这样美好的消息背后,有着一种类型的乳腺癌,让每一位听到它的大夫都愤恨不已,因为这种类型的乳腺癌不仅有着很强的侵犯性和快速的进展性,还对大多数的治疗手段不敏感,尤其在年轻女性与年轻妈妈群体中高发。最可怕的是,这种类型的乳腺癌大都有着不良的预后及再复发的危险。这种类型的乳腺癌正是本文的主角——三阴乳腺癌(Triple-negative breast cancer)。
看完了上面的话,也千万不要被吓到。因为本期《新英格兰杂志》的这篇文章,讲的正是新近发明的一种对付三阴乳腺癌强而有力的武器——PARP抑制剂BSI-201(也就是Iniparib,来自BiPar公司,现在已被sanofi aventis收购。从上次给Anacetrapid命名起,我似乎养成了这个习惯,我们不妨叫这个药为“依尼帕尼”如何:P)。这项II期的临床试验,就验证了Iniparib联合化疗,对转移性三阴乳腺癌的治疗作用。
要了解为什么三阴乳腺癌是乳腺癌中预后较差的一种,我们需要明白“三阴”这个名称的来源。这里的“三阴”指的是三种受体的表达均为阴性(-),这三种受体分别是雌激素受体(estrogen-receptor, ER)、孕激素受体(progesterone-receptor, PR)和人表皮生长因子受体(human epidermal growth factor receptor type 2, HER-2)。由于前两种受体表达阴性,使得这一类型的乳腺癌对于激素治疗不敏感,诸如三苯氧胺(他莫西芬,tamoxifen);而最后一种受体表达阴性,使得其也无法使用赫赛汀(Herceptin)之类的药物进行治疗。总之,“三阴”的名字就因为三种受体均为阴性而得名的。
三阴乳腺癌好发于年轻女性、带有BRCA1突变基因的女性、年轻妈妈以及一些西方人种。其中值得注意的是BRCA1(breast cancer type 1)这个基因,它可以转录产生一种蛋白,导致乳腺癌的易感。这个基因对于我们理解这项研究以及Iniparib这个药物也是有意义的。 之所以说“三阴乳腺癌”虽然预后不好,但并不可怕,是因为一般而言,三阴乳腺癌对于手术之前的新辅助化疗效果比激素受体阳性的乳腺癌是要好的,所以只要发现的及时,也能够达到良好的预后。但如果乳腺癌已经转移,那么预后就会比较差,一般的中位生存期也只有1年左右。而且对于转移性的三阴乳腺癌患者而言,并没有一种行之有效的标准治疗方案,也使得这一领域迫切需要有所突破。
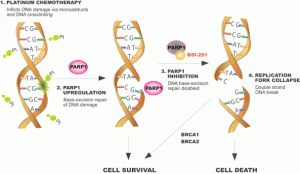
Okay,说完了三阴乳腺癌,我们再来说一说Iniparib,也就是我们命名为依尼帕尼的这个药物。这是一种PARP1(Poly [adenosine diphosphate–ribose] polymerase,二磷酸腺苷核糖多聚酶)的抑制剂。从上面的图可以看出这一种酶是如何发挥作用的。
通常而言,在我们人类体内,每天都进行着大量的DNA的破坏和修复过程,之所以我们能够在日复一日的新陈代谢中保持原有的功能,我们自身的DNA修复功能起到了不可替代的作用。而在众多修复过程之中,PARP就是其中之一,它能够修复受损的DNA,并终止含有不可修复DNA的细胞分裂周期的作用。当然,这些都是在正常的人体细胞中,但如果癌细胞也具备了这样的功能,那情况就大大不同了。试想,如果癌细胞也具备了这样的功能,那么,我们使用的众多化疗药物就会一边破坏着癌细胞的DNA,一边又被其自身修复,总不会达到太好的疗效。在实际情况中,近期的研究表明,的确有癌细胞利用了PARP修复DNA的这一机制在与人类对抗,三阴乳腺癌很可能正是其中之一。
说到这里,应该就容易理解不少了。由于三阴乳腺癌的癌细胞,使用了PARP修复DNA的这一机制,所以我们对其使用这种PARP的抑制剂,就可以阻止其自身修复的机制,达到杀灭癌细胞的目的。而且,不仅仅如此,对于那些BRCA突变或缺陷的患者而言,这一药物更能够特异的对癌细胞产生作用,而对正常细胞的影响相对较小。为了不打断思路,此处的具体机制就先不细说了,可以参考编辑评述文章的相应内容(见本文后的评述内容):)
嗯,基础知识应该就是这样。下面让我们来看一看试验设计以及结果。这是一项II期临床试验,共选取了123位患者。比较的是吉西他滨(gemcitabine,也叫健泽)+顺铂(carboplatin,也叫卡铂)化疗方案联合与不联合使用Iniparib,也就是我们所说的依尼帕尼(PARP1抑制剂),对于转移性三阴乳腺癌的治疗效果。将患者随机分为两组,分别接受吉西他滨(1000 mg/m2, 毫克每平方米体表面积)+卡铂(AUC2,曲线下面积)联合或不联合Iniparib(5.6 mg/kg,毫克每公斤体重),其中前两个药在第1、8天给药,第三个药在1、4、8、11天给药,一个疗程21天。主要的研究终点为临床收益率和安全性。除此之外,在那些接受了交叉给药的单独使用化疗治疗但进展的患者身上,还发现了Iniparib的最小抗肿瘤活性,研究者也提到了之前的同类药物Olaparib(奥拉帕尼)的临床研究,当时也是发表在了NEJM上。可谓开创了PARP抑制剂研究的先河。
试验的结果表明,iniparib组与化疗组还是有着显著差异的。临床收益率分别为56%与34%(p=0.01),总有效率为52%与32%;中位生存期分别为12.3个月与7.7个月。而两组的不良反应率却没有显著的差异。基于这样的结果,研究者也正在进行对总生存期与无进展生存评价的III期试验。
来源:《新英格兰医学杂志》2011-1-20 原始论文 Iniparib plus Chemotherapy in Metastatic Triple-Negative BreastCancer. Joyce O’Shaughnessy, M.D., Cynthia Osborne, M.D., John E. Pippen, M.D., et al. N Engl J Med 2011; 364:205-214January 20, 2011
说完了这项研究,让我们再来看看本期《新英格兰医学杂志》的编辑述评,《PARP与癌症,坐守渔翁之利》对这项研究发表的评论。这篇述评开头还引用了尼采的话,可谓文采飞扬哈。
除了文采以外,个人以为这篇文章可以作为PARP抑制剂治疗癌症研究的一篇短小精悍的导读。作者首先简单介绍了DNA修复的机制,其中包括BRCA1/2突变以及PARP的作用。原始研究的文章中我也提到,PARP抑制剂可以对BRCA突变患者体内的癌细胞产生特异性的作用,具体机制也许可以从这里得出解释。
首先我们来细说BRCA这个基因,比较经典的文章可以阅读这篇Natrue的文章,BRCA1/2是人体内进行DNA双链断裂修复的重要基因,主要修复的是双链断裂的DNA。而这一类修复还有着自身的特点,由于双链断裂大都由于一些致死性的因素,诸如放射线或细胞毒性药物等,修复的机制基本是通过同源染色体的重组,此时BRCA1/2可以精确的调控这一过程,完成DNA的修复。一般而言,带有遗传性BRCA基因突变的患者,通常也有着正常的BRCA的功能,靠得是其中一个正常的等位基因;但是,在这些患者体内的癌细胞中,这一个正常的等位基因往往无法表现出活性,此时他们就只能通过PARP来帮助进行DNA的修复,而我们通过抑制PARP的活性,也就间接的达到了消灭癌细胞的目的。这也正是特异性作用于癌细胞的机制解释。
介绍完机理,这篇述评的作者回顾了PARP抑制剂的研究历程。初始的研究来自于阿斯利康公司的药物临床试验,也就是之前提到过的Olaparib(奥拉帕尼),也发表在了新英格兰上。当时是一项I期的临床试验,并不仅仅针对与乳腺癌,还对卵巢癌、前列腺癌一同进行了研究,但研究都与BRCA基因突变有关。之后,一项II期的研究结果发表在了Lancet上,主要针对进展期的乳腺癌进行了研究,原文在这里。
评述作者充分肯定了该项研究的重大意义,之后,就开始“炮轰”了,hoho。你说PARP与BRCA基因有关,但是在乳腺癌里,BRCA1/2突变相关的仅占不到5%,所以证明对于其他的乳腺癌你是不是也管用就非常重要了。即便三阴乳腺癌在BRCA基因突变患者中高发,但在三阴乳腺癌分型中比例最大的还是基底型(Basal-like),所以在研究过程中检测被试是否带有BRCA突变就很重要,否则我们就不知道PARP抑制剂究竟是如何作用的。这一点这项研究中并没有进行。除此之外,样本量较小、终点是研究者进行评估的(没有设盲)、化疗方案并非传统使用惯例、预后提示基线不平衡等不足之处也一一被指出。
来源:《新英格兰医学杂志》2011-1-20 评论
PARP and Cancer — If It’s Broke, Don’t Fix It. Lisa A. Carey, M.D., and Norman E. Sharpless, M.D. N Engl J Med 2011; 364:277-279. January 20, 2011
个人的一点看法:不知道大家看过之后会有什么感觉。但就我个人而言,有一些欣喜,毕竟又是一项临床上的突破,但更多的还是无奈。尤其在肿瘤学方面,估计无奈总是大于喜悦的,因为我们可以看到,即便说可以改善预后,总的中位生存期也不过延长了5个月。而这类新药,想必售价不菲。在这多出的5个月里,这些患者又会是怎样的一种状态呢。或许,这也是一个问题吧。
p.s. 这也是两周以前美国肿瘤年会上一篇大会发言的报告,曾经刊登在NEJM online first上。我们曾经的“爪闻”就有过报道哈~